- -
- 100%
- +
Tab. 1 Diagnostische Kriterien für gingivale Gesundheit und durch dentale Plaque induzierte Gingivitis4.
Zustand des ParodontsGesundheitGingivitisIntaktes ParodontSondierbarer AttachmentverlustneinneinSondierungstiefen (bei Ausschluss von Pseudotaschen)≤ 3 mm≤ 3 mmBluten auf Sondieren (BOP)< 10 %ja (≥10 %)Röntgenologischer KnochenabbauneinneinReduziertes ParodontKein Parodontitispatient, (z. B. bei fazialen Rezessionen)Sondierbarer AttachmentverlustjajaSondierungstiefen (alle Stellen und bei Ausschluss von Pseudotaschen)≤ 3 mm≤ 3 mmBluten auf Sondieren (BOP)< 10 %ja (≥ 10 %)Röntgenologischer KnochenabbaumöglichmöglichErfolgreich behandelter stabiler ParodontitispatientSondierbarer AttachmentverlustjajaSondierungstiefen (alle Stellen und bei Ausschluss von Pseudotaschen)≤ 4 mm (keine Stelle ≥ 4 mm und BOP)≤ 3 mmBluten auf Sondieren (BOP)< 10 %ja (≥ 10 %)Röntgenologischer KnochenabbaujajaTab. 2 Parodontale und gingivale Gesundheit4.
A. Klinische gingivale Gesundheit bei intaktem ParodontB. Klinische gingivale Gesundheit bei reduziertem Parodonti. Stabiler Parodontitispatientii. Kein ParodontitispatientTab. 3 Gingivitis – durch dentalen Biofilm induziert4.
A. Allein mit dentalem Biofilm assoziiertB. Beeinflusst durch systemische oder lokale Risikofaktoreni. Systemische Risikofaktoren (modifizierende Faktoren)(a) Rauchen(b) Hyperglykämie(c) Ernährungsfaktoren(d) Pharmakologische Wirkstoffe (verordnungspflichtig, nichtverordnungspflichtig, Partydrogen)(e) Geschlechtshormone (Pubertät, Menstruationszyklus, Schwangerschaft, orale Kontrazeptiva)(f) Hämatologische Zuständeii. Lokale Risikofaktoren (prädisponierende Faktoren)(a) Faktoren, die zur Retention dentalen Plaquebiofilms beitragen (z. B. überstehende Restaurationsränder)(b) MundtrockenheitC. Medikamentös induzierte GingivavergrößerungTab. 4 Gingivale Erkrankungen – nicht durch dentalen Biofilm induziert4.
A. Genetische/entwicklungsbedingte Störungeni. Erbliche GingivafibromatoseB. Spezifische Infektioneni. Bakterieller Genese(a) Neisseria gonorhoeae*(b) Treponema pallidum*(c) Mycobacterium tuberculosis*(d) Streptokokken-Gingivitisii. Viraler Genese(a) Coxsackie-Virus (Hand-Fuß-Mund-Krankheit)*(b) Herpes simplex I und II (primär oder rezidivierend)*(c) Varizella zoster (Windpocken und Gürtelrose – Nervus trigeminus)*(d) Molluscum contagiosum(e) Humanes Papillomavirusiii. Fungaler Genese(a) Candidose(b) Andere Mykosen (z. B. Histoplasmose, Aspergillose)C. Entzündliche und Immunzuständei. Überempfindlichkeitsreaktionen(a) Kontaktallergie*(b) Plasmazellgingivitis*(c) Erythema multiforme*ii. Autoimmunerkrankungen von Haut und Schleimhäuten(a) Pemphigus vulgaris*(b) Pemphigoid*(c) Lupus erythematodes* (systemischer LE, diskoider LE)iii. Granulomatös entzündliche Erkrankungen (Orofaziale Granulomatosen)(a) Morbus Crohn*(b) Sarkoidose*D. Reaktive Prozessei. Epuliden(a) Epulis fibrosa (peripheres Fibrom)(b) Kalzifizierendes fibroblastisches Granulom(c) Epulis vascularis (pyogenes Granulom)(d) Peripheres RiesenzellgranulomE. Tumoreni. Präkanzerosen(a) Leukoplakie(b) Erythroplakieii. Maligne Tumore(a) Plattenepithelkarzinom*(b) Leukämische Zellinfiltration*(c) Lymphome* (Hodgkin, Non-Hodgkin)F. Endokrine, Ernährungs- und Stoffwechselerkrankungeni. Vitaminmangel*(a) Vitamin-C-Mangel (Skorbut)G. Traumatische Läsioneni. Physikalisches/mechanisches Trauma(a) Reibungskeratose(b) Mechanisch induzierte Gingivaulzeration(c) Selbstzugefügte Läsionenii. Chemische (toxische) Läsioneniii. Thermische Läsionen(a) GingivaverbrennungenH. Gingivale Pigmentierungeni. Melanoplakieii. Rauchermelanoseiii. Medikamenteninduzierte Pigmentierung (Antimalariamedikamente, Minocyclin)iv. Amalgamtätowierung* systemische Beteiligung oder orale Manifestation systemischer Zustände
Eine Vielzahl spezifischer bakterieller, viraler und mykotischer Infektionen kann sich an der Gingiva manifestieren (Tab. 4).
Die ICD-10 unterscheidet die akute und chronische Gingivitis. Dabei werden die akute nekrotisierende ulzeröse Gingivitis (A69.1) und die Gingivostomatitis herpetica (Herpes simplex; B00.2; s. Tab. 4) in der Systematik nicht den parodontalen, sondern anderen Erkrankungen zugeordnet (Tab. 5)3.
Tab. 5 Gingivitis nach ICD-103.
K05.0 Akute GingivitisK05.1 Chronische GingivitisGingivitis (chronica):– desquamativa– hyperplastica– simplex marginalis– ulcerosao. n. A.Parodontitis
Nekrotisierende Parodontalerkrankungen
Die nekrotisierenden Parodontalerkrankungen haben infektiösen Charakter, aber modifizierende Faktoren, insbesondere eine herabgesetzte Immunantwort, sind entscheidend in der Pathogenese. Mikrobiologisch spielen Spirochäten eine große Rolle, es wurden aber auch P. intermedia, Selemonas- und Fusobacterium-Spezies nachgewiesen. Innerhalb der Läsionen wurden vier Zonen differenziert:
1) die oberflächliche bakterielle,
2) die an neutrophilen Granulozyten reiche,
3) die nekrotische und
4) die spirochätere Infiltrationszone.
Die nekrotisierenden Parodontalerkrankungen (NG: nekrotisierende Gingivitis; NP: nekrotisierende Parodontitis; NS: nekrotisierende Stomatitis; Noma) werden nach folgenden Patientengruppen unterschieden: (a) chronisch, schwer kompromittierte Patienten (HIV-Infektion, AIDS, Immunsuppression, schwere Unterernährung, Virusinfektionen, extreme Lebensbedingungen), (b vorübergehend und/oder moderat kompromittierte Patienten (psychosozialer Stress, Ernährung, Rauchen, Angewohnheiten; Tab. 6). Die Diagnose der nekrotisierenden Parodontalerkrankungen erfolgt nach klinischen Kriterien: Nekrose und Ulkus der Interdentalpapillen (in 94–100 % der Fälle), Zahnfleischbluten (95–100 %), Schmerzen (86–100 %), Ausbildung von Pseudomembranen (73–88 %) und Mundgeruch (84–97 %). Extraorale Symptome sind eine regionäre Lymphadenitis (44–61 %) und seltener Fieber (20–39 %)5. Die ICD-10 listet die akute nekrotisierende ulzeröse Gingivitis unter „Sonstige Spirochätenkrankheiten“ (A65-69) und dort unter „Sonstige Fusospirochätosen“ auf (A69.1)3.
Tab. 6 Nekrotisierende Parodontalerkrankungen (NG: nekrotisierende Gingivitis; NP: nekrotisierende Parodontitis; NS: nekrotisierende Stomatitis; PAR: Parodontium)5,10.
KategoriePatientenPrädisponierende FaktorenKlinischer ZustandChronisch schwer immunkompromittierte PatientenErwachseneHIV+/AIDS mit CD4-Zellzahlen < 200 und nachweisbarer ViruslastNG, NP, NS, Noma (mögliche Progression)Andere schwerwiegende systemische Zustände (Immunsuppression)KinderSchwere MangelernährungExtreme LebensumständeSchwere (virale) InfektionenTemporär und/oder moderat immunkompromittierte PatientenGingivitispatientenUnkontrollierte Faktoren: Stress, Ernährung, Rauchen, HabitsGeneralisierte NG (mögliche Progression zu NP)Frühere nekrotisierende PAR-Erkrankungen, residuale KraterLokale Faktoren: Wurzelengstand, ZahnfehlstellungenLokalisierte NG (mögliche Progression zu NP)Allgemeine prädisponierende Faktoren für nekrotisierende PAR-ErkrankungenNG (nur selten Progression)ParodontitispatientenAllgemeine prädisponierende Faktoren für nekrotisierende PAR-ErkrankungenNP (nur selten Progression)Parodontitis
Bei Belassen der bakteriellen Beläge auf den Zahnoberflächen persistiert die durch den oralen Biofilm induzierte Gingivitis. Dieser Zustand kann bei einigen Menschen über lange Zeiträume unverändert bestehen bleiben, ohne dass es zu Destruktionen kommt, während es bei den meisten später und bei wenigen Menschen früher zur Zerstörungen des Zahnhalteapparats kommt (Parodontitis). Das entscheidende Unterscheidungsmerkmal zwischen Gingivitis und Parodontitis ist die weitgehend irreversible Zerstörung des Zahnhalteapparats, die als Verlust klinischen Attachments und röntgenologischer Knochenabbau festgestellt wird. Beginn, Ausmaß und Geschwindigkeit der Zerstörung können sich von Person zu Person stark unterscheiden. Von 1970 bis 1985 wurde eine Gruppe von Arbeitern auf einer Teeplantage auf Sri Lanka, die praktisch keine Mundhygienemaßnahmen betrieben und deshalb alle Gingivitis hatten, beobachtet: 11 % entwickelten trotz jahrelang bestehender Gingivitis praktisch keine Parodontitis, während bei 81 % nur moderate parodontale Destruktionen festzustellen waren, die sich erst ab dem 40. Lebensjahr manifestierten. Nur 8 % der Teepflücker zeigten schwere Parodontitisverläufe mit rascher Progression bei erheblichen Gewebezerstörungen und Zahnverlust, die zum Großteil schon bei Heranwachsenden einsetzten und bereits bei jungen Erwachsenen zu erheblichen Zahnverlusten führten6.
Die Parodontitis wird nach Schweregrad und Komplexität in vier Stadien unterteilt (Stadium I bis IV; Tab. 7). Primär sollte dafür klinischer Attachmentverlust (CAL) zugrunde gelegt werden, falls dazu keine Angaben vorliegen, röntgenologischer Knochenabbau (Abb. 4a). Dabei kann das Ausmaß als lokalisiert (< 30 % der betroffenen Zähne), generalisiert (≥ 30 % der betroffenen Zähne) oder Molaren-Inzisiven-Muster (s. „lokalisierte aggressive Parodontitis“) beschrieben werden. Im Unterschied zur Klassifikation von 19997 wird nur approximaler klinischer Attachmentverlust berücksichtigt. CAL aufgrund von Rezessionen, die keine entzündliche Pathogenese haben müssen8, bleiben unberücksichtigt. Für die Berechnung des Ausmaßes wird die Zahl der Zähne und nicht die der Stellen zugrunde gelegt (Tab. 7). Nicht nur CAL und Knochenabbau determinieren den Schweregrad, sondern auch durch Parodontitis eingetretener Zahnverlust. Es ist nicht mehr möglich, eine Parodontitis durch Extraktionen in einen niedrigeren Schweregrad zu transferieren. Sondierungstiefen (ST) spielen wieder eine Rolle und markieren zusammen mit BOP (Bluten auf Sondieren) den Unterschied zwischen einem stabilen Zustand nach erfolgreicher Parodontitistherapie (s. Tab. 3 und 4) und Parodontitis (Tab. 7). Entsprechend der Geschwindigkeit der Gewebezerstörung werden drei Progressionsgrade unterschieden: Grad A: langsame Progression, Grad B: moderate Progression, Grad C: rasche Progression (Tab. 8)9,10.
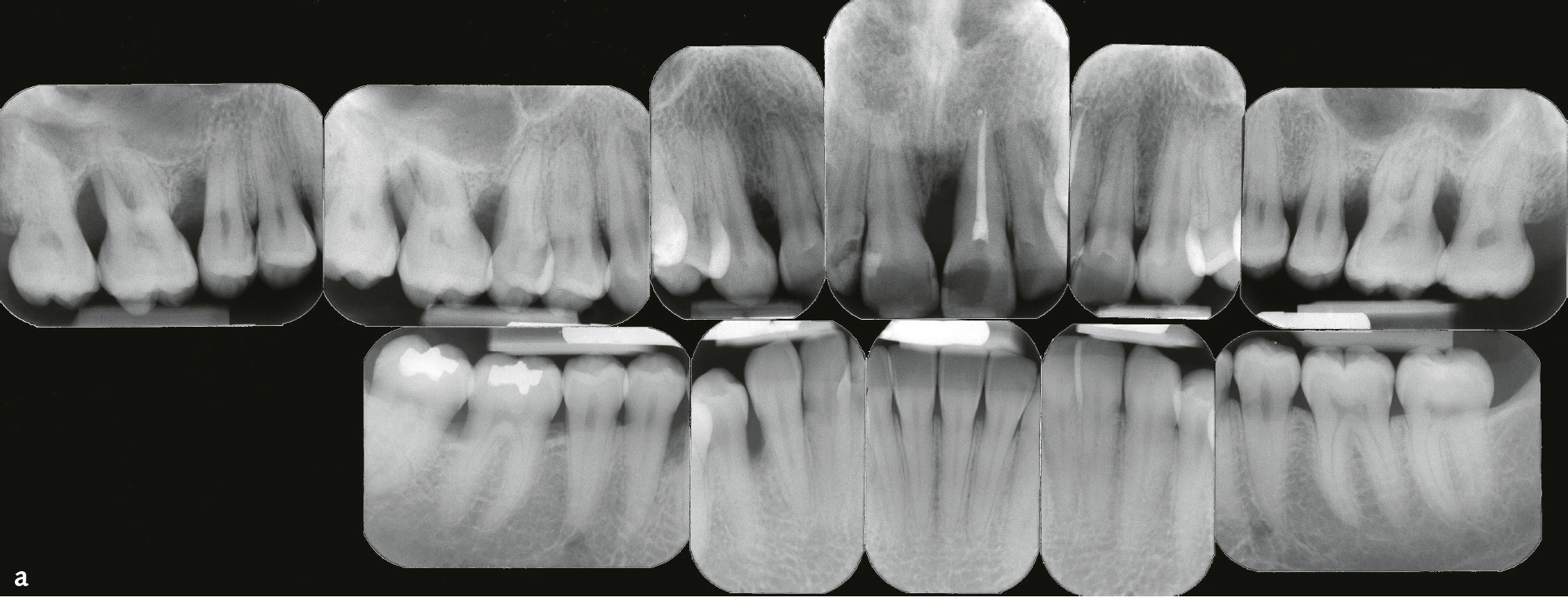
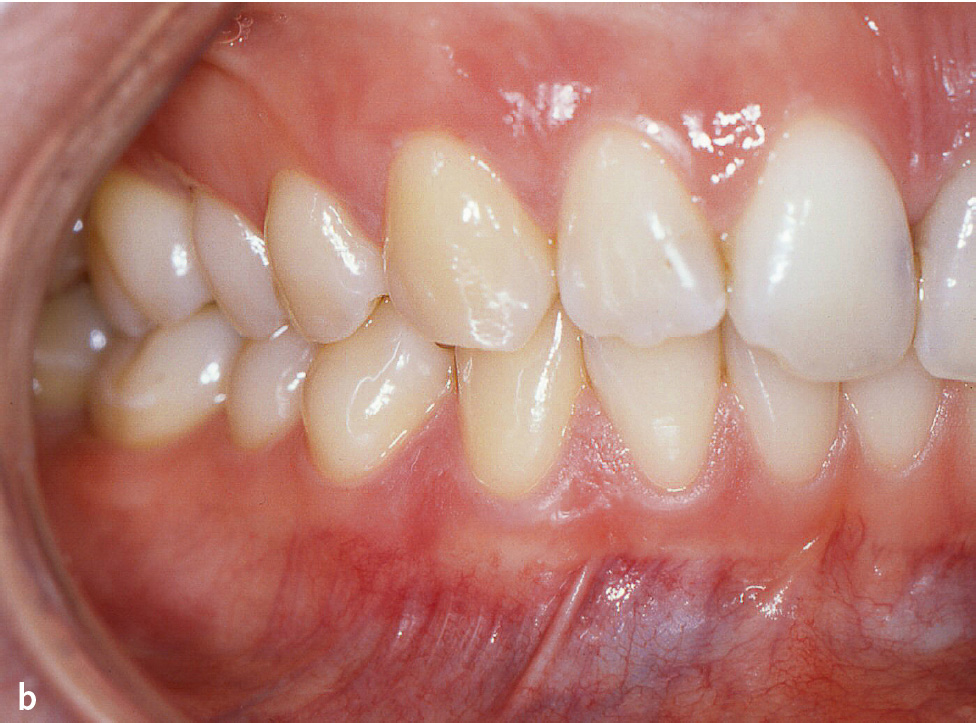
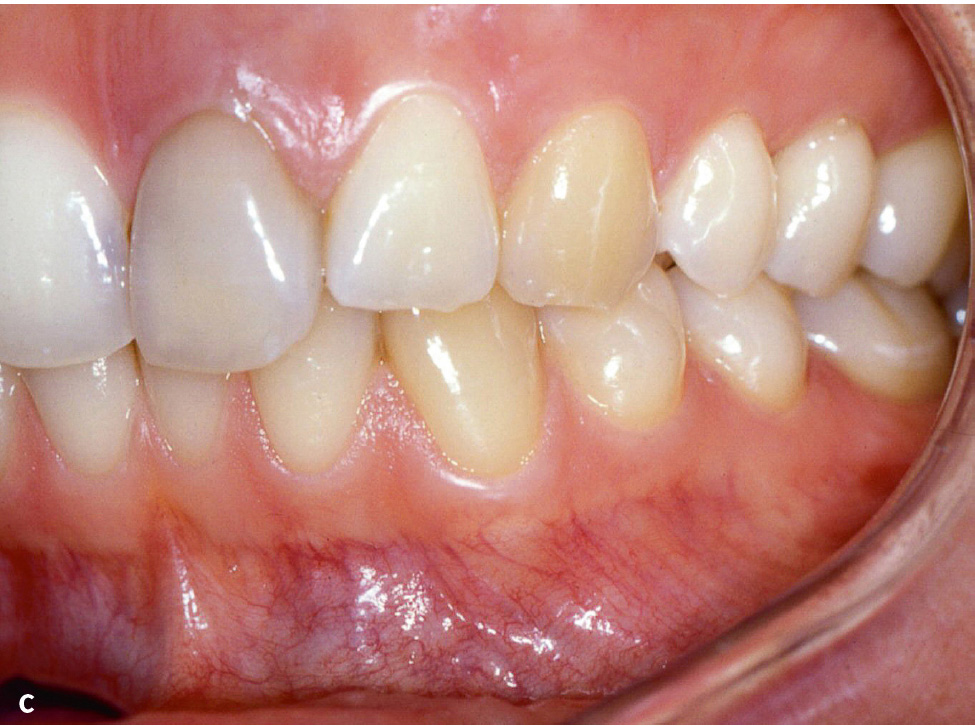
Abb. 4a bis c Patientin im Alter von 24 Jahren mit generalisierter aggressiver Parodontitis18, Parodontitisstadium III (Molaren-Inzisiven-Muster) Grad C. a) Röntgenstatus: Knochenabbau bis ins apikale Wurzeldrittel an den Zähnen 16, 21 und 26 (Stadium III), im Unterkiefer geringerer Knochenabbau bis 50 % der Wurzellänge an Zahn 44, kein Zahnverlust, aber Sondierungstiefen ≥ 6 mm an Zahn 16, Grad-III-Furkationsbeteiligung an Zahn 16 und 26, distal Zahn 16 Knochenabbau 70 % der Wurzellänge (geteilt durch das Lebensalter = 2,9; Grad C). b und c) Klinische Ansicht: keine supragingivale Plaque, Destruktion überschreitet Erwartungen durch Biofilmauflagerungen (Grad C).
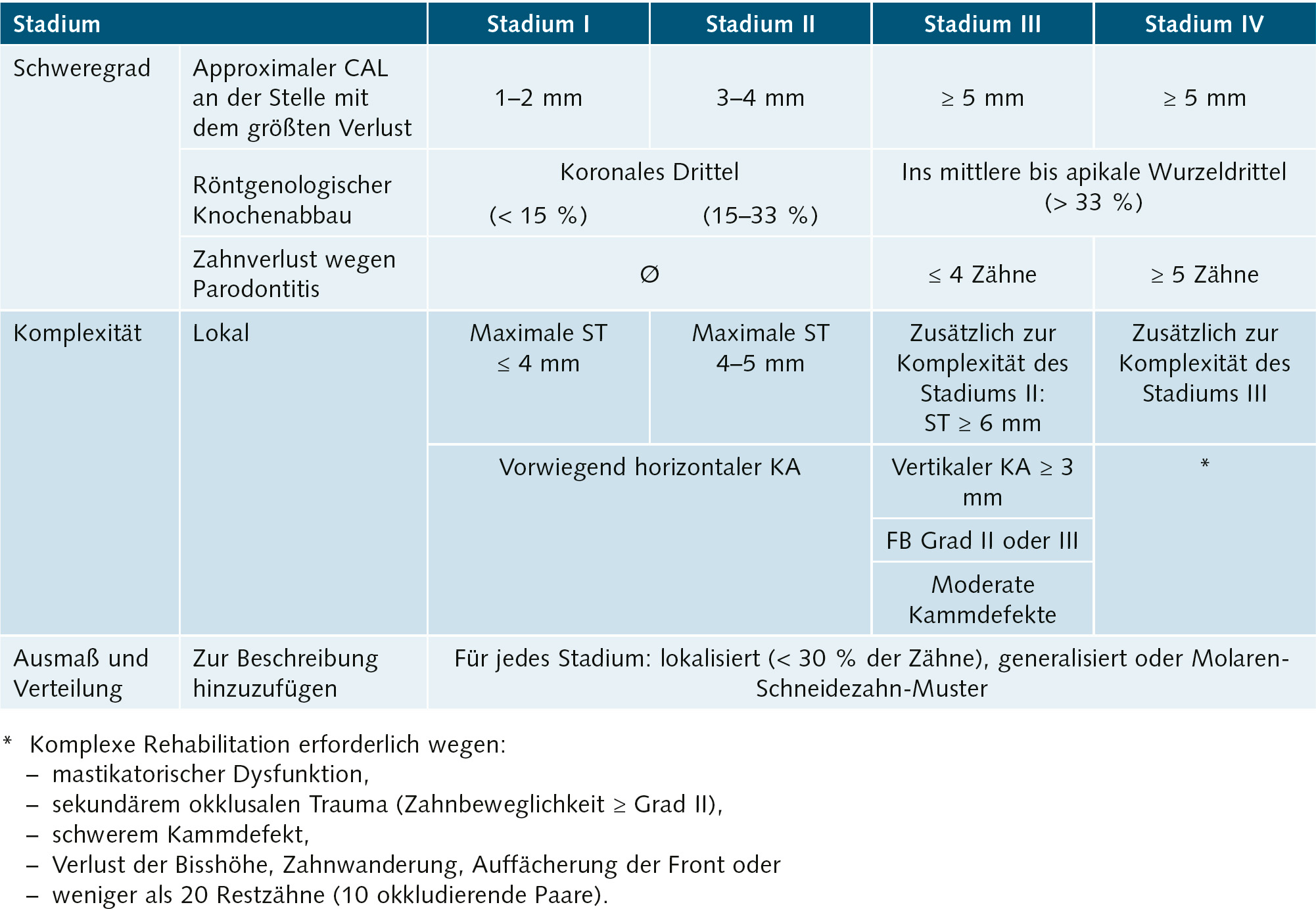
Tab. 7 Klassifikation der Parodontitis: Stadien basierend auf Schweregrad, Komplexität sowie Ausmaß bzw. Verteilung (CAL: klinischer Attachmentverlust; ST: Sondierungstiefe; KA: Knochenabbau; FB: Furkationsbeteiligung)1,9,10.
Tab. 8 Klassifikation der Parodontitis: Grade, die biologische Eigenschaften der Erkrankung widerspiegeln, wie Evidenz von oder Risiko für rasche Progression (CAL: klinischer Attachmentverlust; KA: Knochenabbau)1,9,10.
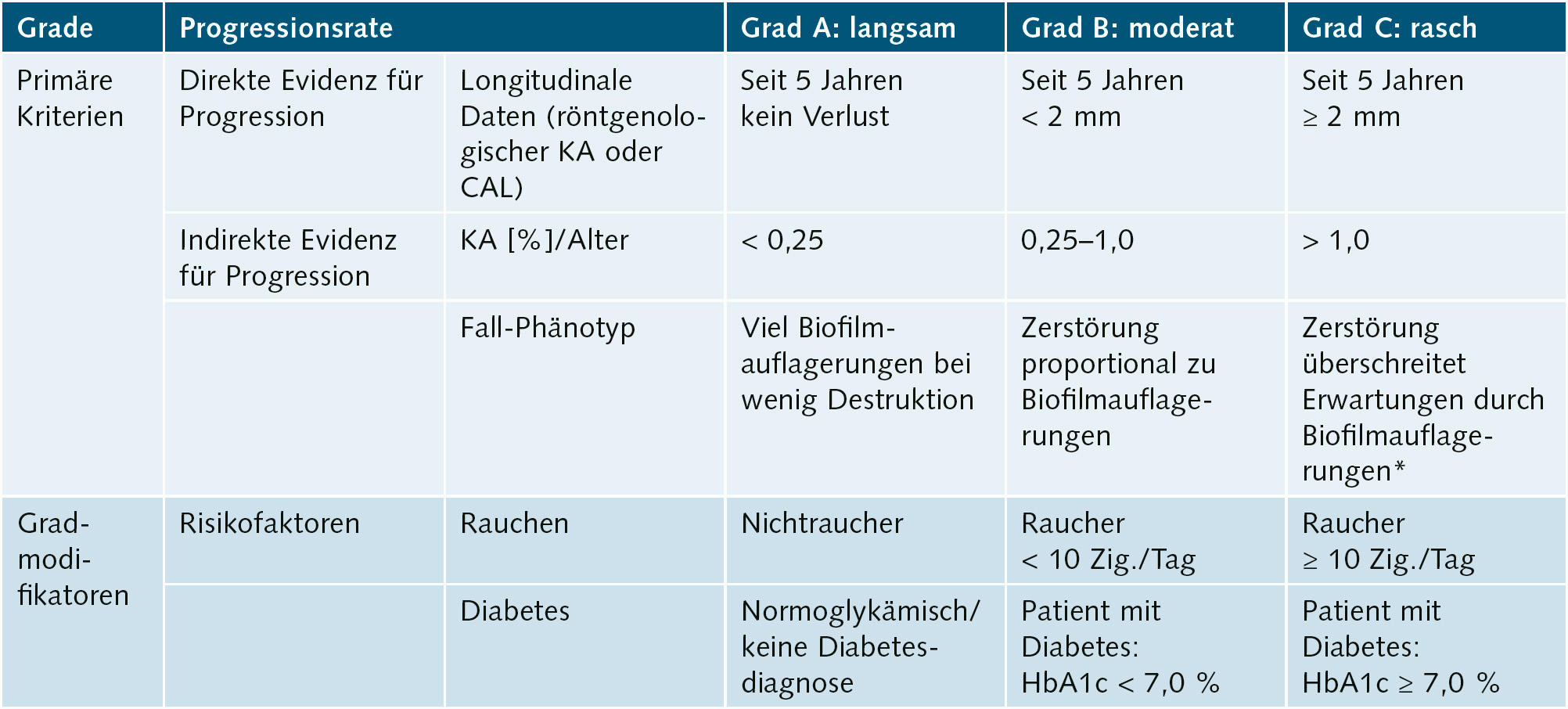
* Spezifische klinische Muster, die Phasen rascher Destruktion und/oder frühes Einsetzen der Erkrankung nahelegen (z. B. Molaren-Inzisiven-Muster; Fehlen eines zu erwartenden Ansprechens auf Standardtherapien zur Infektionskontrolle).
In der ICD-10 kommt Parodontitis noch als Chronische Parodontitis (K05.3) vor. Dazu werden gruppiert: Chronische Perikoronitis, Parodontitis complex, -simplex und -o. n. A. (ohne nähere Angaben). Ferner wird die Diagnose Parodontose (K05.4) aufgelistet. Ausdrücklich wird die „juvenile Parodontose“ eingeschlossen3. Als juvenile Parodontitis wurde ein Großteil der klinischen Bilder vor 1999 bezeichnet, die danach aggressive Parodontitis genannt wurden7. Parodontitis, die bereits bei Kindern und Jugendlichen auftritt, bei der die Zerstörung im Vergleich zum Lebensalter sehr fortgeschritten ist oder mehr Zerstörung festzustellen ist, als der vorhandene Biofilm erklären kann (Abb. 4), werden in der neuen Klassifikation mit einem Grad C gekennzeichnet (hohe Progressionsrate)9,10. Wie kann es sein, dass die ICD-10 für die infektiös-entzündliche Zerstörung des Parodonts eine Wortendung verwendet, die allgemein für degenerative Prozesse verwendet wird (-ose)? In vielen Fällen der Parodontitis mit hoher Progressionsrate besteht ein Missverhältnis zwischen der Menge der bakteriellen Ablagerungen sowie der klinisch sichtbaren Entzündung (Schwellung, Rötung) und dem Ausmaß der Gewebedestruktion. Dies führte dazu, dass der Begriff „Periodontosis/Parodontosis“ zum Teil synonym wie juvenile Parodontitis verwendet wurde11. Darüber hinaus gibt es noch Sonstige Krankheiten des Parodonts (K05.5) und Krankheit des Parodonts, nicht näher bezeichnet (K05.6)3.
Parodontitis als Manifestation von Systemerkrankungen
Viele angeborene (genetische Störungen, z. B. Papillon-Lefèvre-Syndrom)12 oder erworbene Systemerkrankungen wie beispielsweise HIV gehen mit gingivalen (s. Tab. 4) und parodontalen Manifestationen einher. Dabei wird erstmals zwischen Systemerkrankungen, die zu parodontalem Attachmentverlust durch Einfluss auf die parodontale Entzündung (z. B. Defekte der neutrophilen Granulozyten), Erkrankungen der Mundschleimhaut und Gingiva, des Bindegewebes (z. B. Ehlers-DanlosSyndrom Typ IV, VIII), Stoffwechsel- und endokrinen Erkrankungen (z. B. Diabetes mellitus) und Erkrankungen unterschieden, die das Parodont unabhängig von der parodontalen Entzündung zerstören (z. B. Langerhans-Zell-Histiozytose; s. nachfolgenden Abschnitt und Tab. 9). Ebenfalls neu ist, dass psychosozialem Stress und Nikotinabhängigkeit eine eigene Rubrik mit entsprechenden ICD-10-Codes eingeräumt wird10,13. Die neutrophilen Granulozyten haben als erste Verteidigungslinie gegen bakterielle Infektionen eine besondere Bedeutung, deshalb gehen Defekte der Zahl oder Funktion dieser Zellen zumeist mit rasch verlaufenden Formen von Parodontitis einher12. Neben vielen seltenen Erkrankungen machen zahlreiche, auch häufigere Erkrankungen wie Diabetes mellitus Typ 2 oder entzündliche Darmerkrankungen in dieser Kategorie die vielfältigen Wechselwirkungen von Parodontitis und Systemerkrankungen deutlich. Die neue Klassifikation listet zu jeder Systemerkrankung den entsprechenden ICD-10-Code auf. In der ICD-10 stehen hier die Grunderkrankungen im Vordergrund (Tab. 9).
Tab. 9 Systemische Erkrankungen und Zustände mit Auswirkungen auf den Zahnhalteapparat13.
KlassifikationErkrankungenICD-10-Code1Systemische Erkrankung mit wesentlichem Einfluss auf parodontalen Attachmentverlust durch Einfluss auf parodontale Entzündung1.1Genetische Erkrankungen1.1.1.Erkrankungen mit immunologischen FunktionsstörungenDown-Syndrom (Trisomie 21)Q90.9Leukozyten-Adhäsionsdefekt-SyndromD72.0Papillon-Lefèvre-SyndromQ82.8Haim-Munk-SyndromQ82.8Chediak-Higashi-SyndromE70.3Schwere Neutropenien– Kongenitale Neutropenie (Kostmann-Syndrom)D70.0– Zyklische NeutropenieD70.4Primäre Immunschwächeerkrankungen– Chronische GranulomatoseD71.0– Hyperimmunoglobulin-E-SyndromD82.9Cohen-SyndromQ87.81.1.2.Erkrankungen der Mundschleimhaut und der GingivaEpidermolysis bullosa– Epidermolysis bullosa dystrophicaQ81.2– Kindler-SyndromQ81.8PlasminogenmangelD68.21.1.3.Erkrankungen der BindegewebesEhlers-Danlos-Syndrom (Typ IV, VIII)Q79.6Angioödem (C1-Inhibitormangel)D84.1Systemischer Lupus erythematodesM32.91.1.4.Stoffwechsel- und endokrine ErkrankungenGlykogenspeicher-SyndromE74.0Gaucher-KrankheitE75.2HypophosphatasieE83.30Hypophosphatämische RachitisE83.31Hajdu-Cheney-SyndromQ78.81.2.Erworbene ImmundefekteErworbene NeutropenieD70.9HIV-InfektionB241.3.Entzündliche ErkrankungenEpidermolysis bullosa acquisitaL12.3Entzündliche DarmerkrankungenK50, K51.9, K52.9Arthritis (rheumatoide Arthritis, Osteoarthritis)M05, M06, M15-M192Andere systemische Erkrankungen mit Einfluss auf die Pathogenese parodontaler ErkrankungenDiabetes mellitus– Typ 1E10– Typ 2E112Andere systemische Erkrankungen mit Einfluss auf die Pathogenese parodontaler ErkrankungenÜbergewicht (Adipositas)E66.9OsteoporoseM81.9Emotionaler Stress und DepressionF32.9Rauchen (Nikotinabhängigkeit)F173Systemische Erkrankungen, die unabhängig von Parodontitis parodontalen Attachmentverlust verursachen können3.1.TumorePrimäre Tumorerkrankungen der parodontalen Gewebe– Orales PlattenepithelkarzinomC03.0-1– Odontogene TumorenD48.0– Andere primäre Tumoren der parodonta len GewebeC41.0Sekundäre metastatische Tumore der parodontalen GewebeC06.83.2.Andere Erkrankungen der parodontalen GewebeGranulomatose mit PolyangiitisM31.3Langerhans-Zell-HistiozytoseC96.6RiesenzellgranulomeK10.1HyperparathyroidismusE21.0Systemische Sklerose (Sklerodermie)M34.9„vanishing bone disease“ (Gorham-Stout-Syndrom)M89.5Andere das Parodont betreffende Zustände
Systemische Erkrankungen und Zustände mit Auswirkungen auf den Zahnhalteapparat
Bestimmte systemische Erkrankungen wie z. B. ein orales Plattenepithelkarzinom können den Zahnhalteapparat zerstören, ohne dass durch den oralen Biofilm induzierte Entzündungsprozesse dabei eine vorrangige Rolle spielen (Tab. 9). Die Pathogenese der parodontalen Zerstörung ist bei diesen Erkrankungen völlig anders als bei der biofilminduzierten Parodontitis.
Parodontale Abszesse und Endo-Paro-Läsionen
Parodontalabszesse (Abb. 5, Tab. 10) und Endo-Paro-Läsionen gehören neben den nekrotisierenden Parodontalerkrankungen zu den wenigen Parodontalerkrankungen, die Schmerzen verursachen. Beide Arten von Läsionen gehen mit sehr rascher Gewebezerstörung einher und erfordern deshalb unmittelbares therapeutisches Handeln. Neben Schmerzen werden als Symptome häufig Empfindlichkeit der Gingiva, Schwellung und Anhebung des Zahnes berichtet. Parodontalabszesse können bei Patienten mit unbehandelter Parodontitis oder nach Therapie, aber auch bei Patienten, die keine Parodontitis haben, auftreten (s. Tab. 10)5.
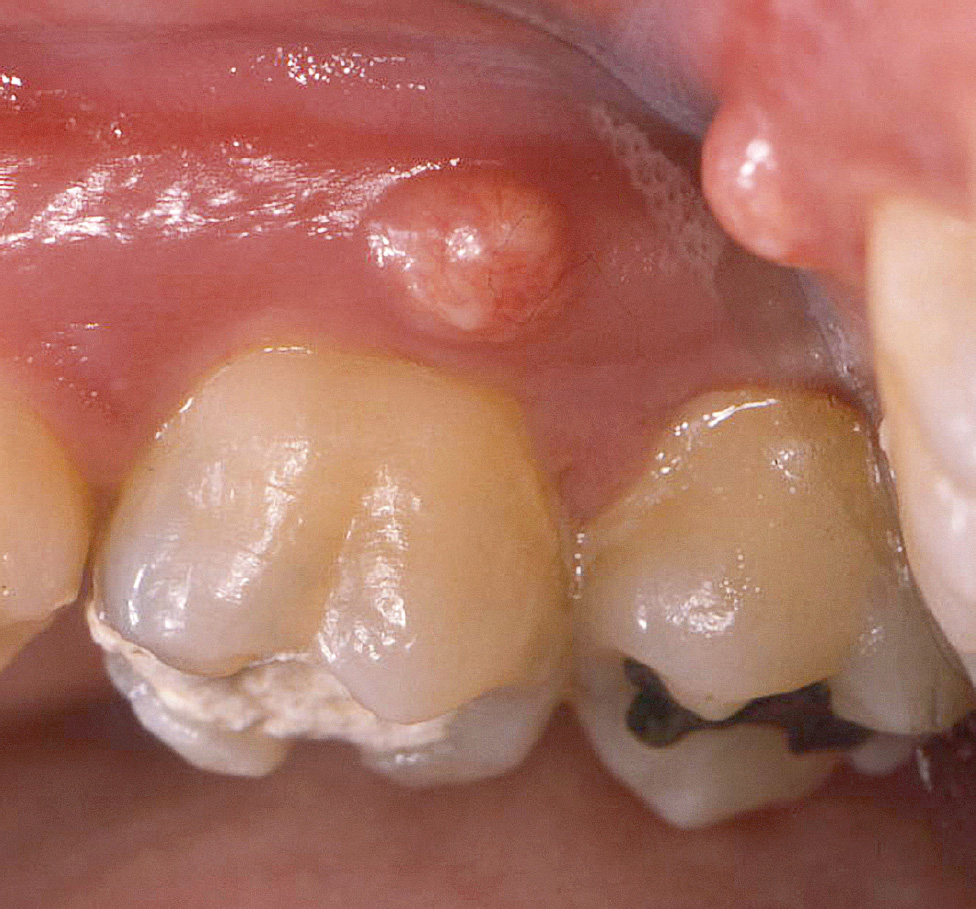
Abb. 5 Parodontalabszess, ausgehend von einer durchgängigen Furkation an Zahn 16.
Tab. 10 Parodontalabszesse (PA)5.
PA bei Parodontitis (in einer bestehenden Tasche)Akute ExazerbationUnbehandelte ParodontitisParodontitis, die nicht auf Therapie ansprichtUnterstützende ParodontitistherapieNach TherapieNach subgingivaler Instrumentierung Nach ParodontalchirurgieNach Einnahme von MedikamentenSystemische Antibiotika Andere Medikamente (z. B. Nifedipin)PA bei Patienten ohne Parodontitis (es muss keine Tasche bestehen)ImpaktionZahnseide, orthodontische elastische Bänder, Zahnstocher, Kofferdam, PopkornhülsenSchädliche GewohnheitenDraht- oder NagelkauenOrthodontische FaktorenEinwirken von orthodontischen Kräften oder KreuzbissGingivawucherungVeränderungen der WurzeloberflächeSchwere anatomische VeränderungenDens invaginatus, evaginatus, OdontodysplasieGeringe anatomische VeränderungenZementwülste, Schmelzparaplasien, FurchenIatrogene ZuständePerforationenSchwere WurzelbeschädigungRiss oder Fraktur, „cracked tooth syndrome“Externe WurzelresorptionDen Endo-Paro-Läsionen ist ein eigener Beitrag in diesem Buch (Beitrag 7) gewidmet14.
Mukogingivale Deformitäten und Zustände
Eine Rezession ist definiert als die apikale Verlagerung des Gingivarands (s. Abb. 3c). Daraus können Beeinträchtigungen der Ästhetik, Dentinhypersensibilität, Karies bzw. nicht kariöse zervikale Läsionen entstehen. Eine aktuelle Klassifikation unterscheidet8,15:
Rezession Typ 1 (RT1; s. Abb. 3c): gingivale Rezession ohne approximalen Attachmentverlust. Die approximale Schmelz-Zement-Grenze (SZG) ist klinisch weder mesial noch distal feststellbar.
Rezession Typ 2 (RT2): gingivale Rezession mit approximalem Attachmentverlust. Das Ausmaß des approximalen Attachmentverlusts (gemessen von der SZG zum Boden der approximalen Tasche) ist geringer bzw. gleich dem bukkalen Attachmentverlust.
Rezession Typ 3 (RT3): gingivale Rezession mit approximalem Attachmentverlust. Das Ausmaß des approximalen Attachmentverlusts (gemessen von der SZG zum Boden der approximalen Tasche) ist größer als der bukkale Attachmentverlust.
Die Identifizierbarkeit der SZG und eine Stufe zwischen Zahnhals und Schmelz können Diagnostik und Therapie von Rezessionen erschweren. Deshalb kann die Klassifikation wie folgt ergänzt werden8:
A– SZG identifizierbar, keine Stufe
A+ SZG identifizierbar, Stufe
B– SZG nicht identifizierbar, keine Stufe
B+ SZG nicht identifizierbar, Stufe
In der ICD-10 werden diese Erkrankungen und Zustände am ehesten unter „Sonstige Krankheiten des Parodonts“ (K05.5) und „Krankheit des Parodonts, nicht näher bezeichnet“ (K05.6) erfasst3.
Traumatische okklusale Kräfte
Traumatische okklusale Kräfte sind definiert als jegliche Kaukräfte, die Zähne und/oder das Parodont schädigen. Hinweise für traumatische Kaukräfte sind Zahnbeweglichkeit, Temperaturempfindlichkeit, extreme Abnutzung der Kauflächen, Zahnwanderung, Beschwerden beim Kauen, Zahnfrakturen, röntgenologisch erweiterter Parodontalspalt, Wurzelresorptionen und Hyperzementose. Unter dem Begriff „okklusales Trauma“ werden unterschieden:
primäres okklusales Trauma (betrifft das intakte Parodont),
sekundäres okklusales Trauma (betrifft das reduzierte Parodont) und
orthodontische Kräfte.
Es gibt keine Hinweise, dass traumatische Kaukräfte oder okklusales Trauma parodontalen Attachmentverlust verursachen können. Auch ergaben Beobachtungsstudien keine Hinweise, dass Kaukräfte Rezessionen verursachen können15.
Zahn- und zahnersatzbezogene Faktoren
Der Begriff der biologischen Breite wird durch suprakrestales befestigtes Gewebe ersetzt. Dieses besteht aus dem Saumepithel und dem suprakrestalen Faserapparat. Veränderte passive Eruption ist ein entwicklungsbedingter Zustand, bei dem der Gingivarand und manchmal auch der Alveolarknochen weiter koronal lokalisiert sind als normal. Sowohl lokalisierte zahnbezogene als auch lokalisierte zahnersatzbezogene Faktoren können plaqueinduzierte Gingivaerkrankungen/Parodontitis modifizieren oder dafür prädisponieren (Tab. 11)15.




